LE BREVET DE PAUL HEROULT
On produit aujourd’hui annuellement plus de 30 millions de tonnes d’aluminium dans le monde. Toutes sont fabriquées par électrolyse, selon le procédé faisant l’objet d’un brevet accordé à Paul Louis Toussaint Héroult en 1886. C’est dire que ce brevet est le texte fondateur de l’industrie de l’aluminium. Il revendique la préparation d’aluminium par l’électrolyse d’alumine en solution dans un bain de cryolithe fondue (fluorure double d’aluminium et de sodium Na3AlF6). L’alumine se décompose en aluminium et oxygène suivant la réaction : .

Figure 1 : timbre français consacré à Paul Héroult, 1986.
On reconnaît à gauche la réaction d’électrolyse de l’alumine, et en bas à droite la schéma du creuset, issu du brevet.
Le procédé est décrit dans le brevet en des termes d’une précision remarquable qui n’ont pas vieilli en dépit des années écoulées et des évolutions de la technologie :
En principe, le procédé que je désire breveter pour la préparation de l’aluminium consiste à décomposer de l’alumine en dissolution dans un bain de cryolithe en fusion par un courant électrique aboutissant au bain, d’une part, au moyen d’une électrode en contact avec le creuset en charbon aggloméré qui contient la cryolithe et, d’autre part, au moyen d’une autre électrode en charbon aggloméré comme la première, plongeant dans le bain. Cette combinaison produit la décomposition de l’alumine en employant un courant de faible tension : l’oxygène se rend à l’anode et brûle avec elle, l’aluminium se dépose sur les parois du creuset qui constitue la cathode, et se précipite en culot dans le fond du creuset. Le bain reste constant et sert indéfiniment s’il est alimenté en alumine. L’électrode positive, c’est-à-dire l’anode, est à remplacer après combustion…
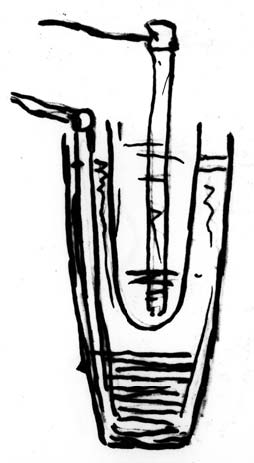
Figure 2 : Première idée d’un dispositif expérimental pour préparer l’aluminium par électrolyse. Croquis de Paul Héroult tracé sur un de ses cahiers de cours, à l’École des mines, en 1883 (trois ans avant le dépôt du brevet).
Le brevet a été déposé en France le 23 avril 1886, accordé le 1er septembre 1886, pour une durée de quinze ans, sous le numéro 175711.
Il a été complété par un certificat d’addition déposé le 15 avril 1887, relatif à la fabrication directe d’alliages d’aluminium et de cuivre, fer ou silicium. Ce certificat précise : «Le courant électrique produit assez de chaleur pour tenir l’alumine en fusion », ce qui est une des caractéristiques importantes du procédé.
L’origine du terme aluminium : du corps composé au corps simple
L’alun (du grec alos, sel) est chronologiquement le premier minerai d’aluminium. C’est un sulfate double d’aluminium et de potassium, dont on tirera l’alumine.
L’alun est connu de longue date. Il est utilisé comme médicament en Chine au XXXVIè siècle avant JC. Pline l’ancien, dans son Histoire naturelle, vers 50 après JC, lui consacre un article qui cite trente-neuf applications sanitaires ou médicales (notamment les pierres d’alun, à usage de déodorant ou baume de rasage) ; il indique son utilisation pour la préparation des cuirs et des laines.
L’alun – comme la plupart des terres – a été considéré longtemps comme un élément indissociable. Cependant, en 1754, Marggraff, chimiste de Berlin, montre qu’il est composé de l’acide du vitriol [acide sulfurique] et d’une terre, qu’il arrive à séparer. Il étudie longuement cette terre d’alun, à laquelle Guyton de Morveau, collaborateur de Lavoisier, donne en 1787 le nom d’alumine (du latin alumen, pour l’alun) dans la nouvelle et monumentale nomenclature chimique qu’il met en place avec Lavoisier, de Fourcroy, Berthollet. En 1807, Humphrey Davy, chimiste et physicien anglais (1778-1829) tente de décomposer l’alumine entre deux électrodes alimentées par une pile de Volta. Cette méthode vient de lui permettre d’isoler les bases de la potasse et de la soude. « Potassium et sodium sont les noms que je me suis risqué à proposer pour les deux nouveaux corps », écrit-il. L’alumine résiste à ce traitement, mais il n’empêche, Davy baptise « aluminium » le métal qu’il n’a pas isolé.
Le nom aluminium est dérivé d’alun. Comme souvent, le corps pur est connu bien après les substances composées dans lesquelles il intervient.
QUERELLE DE BREVETS ENTRE PAUL HEROULT ET CHARLES MARTIN HALL
Un brevet très voisin de celui de Paul Héroult a été déposé par Charles Martin Hall le 9 juillet 1886 aux Etats-Unis et le 2 avril 1889 en France, où ces nouvelles demandes ne soulèvent pas de problème particulier. La législation française voulant que l’invention soit attribuée au premier déposant, seul le brevet de Paul Héroult est valable. Mais il n’en va pas de même aux Etats-Unis, où apparaît une « querelle de brevets » entre les deux inventeurs. La législation américaine veut que le brevet soit attribué à celui des deux inventeurs qui a le premier réalisé et mis en pratique son invention. Les premiers essais de Hall datant du début de 1886 et ceux de Héroult de 1885, c’est encore celui-ci qui aurait dû l’emporter. Mais la loi des États-Unis comporte une clause qui favorise les inventeurs américains : elle exige que les dates de réalisation et de mise en pratique soient établies sur le territoire des États-Unis. Héroult n’ayant pas pu remplir cette condition pour ses expériences de 1885, c’est à Hall qu’a été attribué le brevet aux Etats-Unis, après une longue procédure, le 2 février 1892.
Finalement, le différend se régla par un compromis entre les deux inventeurs, Héroult ayant accepté de limiter l’exploitation de son brevet à l’Europe, et Hall à l’Amérique
(1).
L’ALUMINIUM PAR LA PILE
Robert Wilhelm Bunsen et Henri Sainte-Claire Deville
(2) (3), ont été les premiers à obtenir, à peu près simultanément, en 1854, de l’aluminium par électrolyse ignée, c'est-à-dire par électrolyse d’un sel fondu, en l’occurrence le chlorure double d’aluminium et de sodium (AlCl3, NaCl). Bunsen avait, en 1852 préparé du magnésium par électrolyse du chlorure fondu de ce métal
(4): il est ainsi le créateur de l’électrolyse ignée. Sainte-Claire Deville, qui avait découvert, au début de 1854, les propriétés de l’aluminium pur et pressenti l’avenir de ce métal
(5), recherchait un moyen économique pour le préparer. L’un et l’autre utilisèrent comme bain pour l’électrolyse le chlorure double d’aluminium et de sodium. Le chlorure d’aluminium (AlCl
3) ne convenait pas, car il se volatilise sans fondre vers 200° C. Le chlorure double AlCl
4Na, au contraire, solide à la température ambiante, fond vers 200° C et ne se volatilise qu’à température beaucoup plus élevée. Le courant électrique était fourni par une pile au zinc et l’aluminium obtenu revenait très cher en raison du coût du zinc consommé. C’est pourquoi Sainte-Claire Deville, pour le procédé industriel qu’il voulait développer, exclut l’électrolyse et retint le procédé chimique de réduction du chlorure double d’aluminium et de sodium par le sodium
(6), dérivé de celui proposé par Wöhler en 1827
(7). On relève cependant, dans une note de Sainte-Claire Deville aux
Comptes rendus de l’Académie des Sciences du 10 décembre 1855
(8), des observations qui montrent que l’auteur était tout près de découvrir, trente ans avant Paul Héroult, le procédé électrolytique partant de l’alumine et non pas du chlorure double d’aluminium et de sodium. Il écrit :
J’ai pu souvent constater la propriété toute spéciale des fluorures alcalins qui en fait un dissolvant presque général à haute température
Sainte-Claire Deville fait passer du courant dans un mélange de fluorures de potassium et de sodium contenant de l’alumine en solution et il constate :
C’est du sodium qui vient brûler au pôle négatif et du fluor qui se dégage au pôle positif.
Malheureusement, il ne fait pas la même expérience avec le fluorure double d’aluminium et de sodium (la cryolithe), qui l’aurait conduit à la découverte : ce sera celle de Paul Héroult.

Figure 3 : Portrait de Paul Héroult, 1888.
PAUL LOUIS TOUSSAINT HEROULT : LA DECOUVERTE A 23 ANS
Héroult est né le 10 avril 1863 dans un petit village de la vallée de l’Orne, Thury Harcourt, où son père exploitait une tannerie. Pendant la guerre de 1870, il séjourne en Angleterre, chez son grand-père, puis est élève au lycée de Caen et, lorsque son père transporte sa tannerie sur les bords de la Bièvre, à Gentilly, au collège Sainte-Barbe à Paris. Il y montre un goût prononcé pour la physique, la chimie et la mécanique, et se fait remarquer par les inventions qu’il imagine, aussitôt traduites par un croquis dans un coin de page. C’est au collège Sainte-Barbe, à l’âge de quinze ans, qu’il lit le livre de Sainte-Claire Deville,
De l’aluminium
(9). Ce livre le passionne, et dans les années qui suivent, l’idée de l’invention qu’il entrevoit se précise peu à peu et ne le lâche plus. Depuis 1860, la Compagnie des produits chimiques d’Alais
(10) et de la Camargue (PCAC), fabrique de l’aluminium à Salindres (Gard) par le procédé chimique de Henri Sainte-Claire Deville (réduction du chlorure double d’aluminium et de sodium par le sodium). Elle est à peu près la seule au monde à produire le nouveau métal. Mais le prix de celui-ci reste élevé, les applications ne progressent pas, la production stagne
(11). Paul Héroult le sait, comme il sait que, grâce à l’invention de la dynamo par Zénobe Gramme (1826-1901), on dispose à partir de 1870 d’énergie électrique à bon marché. Héroult n’ignore pas que c’est en raison du coût de l’électricité que Sainte-Claire Deville n’a pas retenu l’électrolyse à l’époque, et il a la conviction que c’est par là que passe l’avenir de l’industrie de l’aluminium. Le procédé reste à trouver. En 1881, alors qu’il prépare le concours d’entrée à l’Ecole des mines, il écrit à sa mère :
Parlons de choses sérieuses. Je suis tourmenté de mon idée d’hier midi et je voudrais faire des essais en grand. Je n’ai pas la tête à ce que je fais. J’en aurais pourtant bien besoin. La théorie me promet la réussite, mes essais de Gentilly aussi. D’un autre côté, cela peut être trouvé d’un jour à l’autre par un autre, et par conséquent perdu pour moi. Toujours je veux en parler sérieusement à papa et toujours je suis arrêté par la peur de me faire moquer de moi […] C’est une affaire à gagner beaucoup.
Paul Héroult entre à l’Ecole des mines en 1882, mais le régime régulier de cours et d’examens comme la discipline et les exigences de l’Ecole ne lui conviennent pas. Il lui faut plus de liberté, et d’abord celle de s’occuper de l’électrolyse de l’aluminium (on trouve sur un de ses cahiers de cours un premier schéma de son invention, fig. 2). Il est renvoyé à la fin de la première année.
Vers 1885, après son service militaire, il entreprend enfin des essais suivis dans la tannerie familiale de Gentilly. Celle-ci, bien qu’arrêtée depuis le décès de son père, a encore un moteur à vapeur en état de fonctionnement et Héroult y dispose d’une petite dynamo Gramme. Il fait de nombreux essais ; il expérimente autour d’idées originales et il vérifie aussi tout ce qu’a écrit Sainte-Claire Deville. Parmi de nombreux fondants, il essaie finalement la cryolithe qu’il tente d’électrolyser. Dans le paragraphe qu’il consacre à «
l’électrolyse par la pile (13) », Sainte-Claire Deville, après avoir indiqué comment on peut recouvrir d’aluminium une cathode de cuivre dans un bain de chlorure double d’aluminium et de sodium fondu, poursuivait :
La cryolithe peut également servir à cette opération, mais elle doit être rendue très fusible par son mélange avec un peu de chlorure double d’aluminium et de sodium […]
Héroult constate en effet que la température nécessaire pour fondre la cryolithe est très élevée et, pour abaisser cette température, il ajoute, comme le recommande Sainte-Claire Deville, du chlorure double d’aluminium et de sodium. Un heureux hasard le conduit au succès. Il le décrit lui-même, quinze ans plus tard, en ces termes :
J’eus la surprise de constater que l’anode en charbon portait des traces évidentes de corrosion. J’en conclus que j’avais eu à faire à un oxyde dont la réduction s’était opérée aux dépens de l’anode. Vérification faite, il se trouva que ce que j’avais acheté pour du chlorure double était en réalité de l’alumine provenant de la décomposition dudit chlorure par l’humidité.
Héroult a donc obtenu de l’aluminium par réduction d’alumine en solution dans la cryolithe. Il ajoute :
De là au procédé actuellement suivi pour la fabrication de l’aluminium, il n’y avait qu’un pas. Ce pas fut néanmoins difficile à franchir, et l’histoire détaillée de l’époque qui suivit serait fastidieuse.
On notera la modestie et la franchise de Paul Héroult dans ce récit. Mais verra-t-on assez le génie qu’il a eu et la compétence dont il a fait preuve dans l’observation, l’analyse et l’interprétation des faits expérimentaux, puis la persévérance que de plus il lui a fallu pour arriver à un procédé brevetable pour la préparation de l’aluminium ?
LA MISE EN ŒUVRE DU PROCEDE
Le brevet obtenu, Héroult veut l’exploiter :
Mes connaissances en chimie étaient limitées à ce que peut savoir un étudiant de 23 ans non spécialiste. Il n’est pas étonnant, dans ces conditions, que […] j’aie cherché appui auprès de personnes faisant autorité dans la matière. M. Pechiney, de Salindres, auquel je proposai mon affaire, me dit : « L’aluminium est un métal à débouchés restreints, il s’emploie pour faire des tubes de lorgnettes, et que vous le vendiez 10 francs ou 100 francs le kilo, vous n’en vendrez pas un kilo de plus. Si vous faisiez du bronze d’aluminium
(15), ce serait une autre affaire, car il s’emploie des quantités considérables de bronze, et si vous en faisiez à bon marché, nul doute que l’affaire ne soit intéressante
(16).
A. R. Pechiney était le gérant de la Compagnie des produits chimiques d’Alais et de la Camargue (PCAC) qui détenait, depuis 1860, comme nous l’avons vu, le quasi-monopole mondial de la fabrication de l’aluminium par le procédé chimique de Sainte-Claire Deville. Il ne semble pas avoir eu la moindre hésitation à rejeter le procédé électrolytique d’avenir que lui proposait Paul Héroult : car l’aluminium tardait à se développer. On en fabriquait 1 à 2 tonnes par an. Il valait 80 F le kg. Il ne représentait guère que 6 à 7 % du chiffre d’affaires de PCAC
(17). Les ventes et la production progressaient peu ; aucun marché d’envergure n’était en vue
(18). Il faut ajouter que, pour suivre Paul Héroult, il fallait d’abord disposer d’énergie électrique en abondance, et que c’était là une aventure dans laquelle Pechiney ne souhaitait pas s’engager : il n’aimait pas l’électricité
(19).
Une histoire de Pechiney à Salindres
Dans le cadre de la Société des produits chimiques d’Alais et de la Camargue (PCAC) qu’il a fondée en 1855, Henry Merle a créé la même année à Salindres (Gard) une soudière, qui est l’ancêtre de la Compagnie Pechiney. C’est là, à proximité des matières premières nécessaires, qu’en 1860 est implanté le procédé chimique de production d’aluminium de Sainte-Claire Deville, en fonctionnement depuis 1857 à Nanterre. Lorsque Henry Merle meurt prématurément en 1877, c’est le directeur de l’usine de Salindres, Alfred Rangod Pechiney (1833-1916), qui lui succède comme gérant de la Société. Il va conduire pendant un tiers de siècle le développement technique et commercial de la Société, dont les principales productions sont l’acide sulfurique, la soude et leurs dérivés. L’aluminium y tient une modeste place, mais c’est à peu près la seule production au monde du nouveau métal, dont Pechiney est seul responsable pendant une quinzaine d’années… avant d’être aussi seul responsable de l’absence de PCAC dans les débuts de l’aluminium électrolytique. Pris de regrets devant le succès du nouveau procédé, il rachète l’usine de Calypso à Saint-Michel–de-Maurienne, en 1895, un revirement stratégique qui permettra plus tard à la compagnie de redevenir un acteur majeur de l’industrie de l’aluminium. En 1950, la Compagnie de produits chimiques et électrométallurgiques d’Alais, Froges et Camargue, héritière de PCAC, prendra le nom de Pechiney, compagnie de produits chimiques et électrométallurgiques.

Figure 4 : Document commercial de Alais, Froges et Camargue, années 1940-1950.
Dans un premier temps, Paul Héroult suit le conseil d’ A.R.Pechiney de fabriquer du bronze d’aluminium : il dépose d’abord un certificat d’addition à son brevet (certificat délivré en septembre 1887, voir deuxième partie du texte BibNum), puis se rend en Suisse où, pour le compte de la Société métallurgique suisse à Neuhausen il produit du bronze d’aluminium. Mais «
ayant compris à la fin que là n’était pas le nœud de la question, mais bien dans l’aluminium pur (20) », il revient en France, à Froges (Isère), où, dans le cadre de la Société électrométallurgique française (SEMF) créée en 1888, il met en place la production d’aluminium pur. Elle démarre à la fin de 1889, avec toutes les difficultés inhérentes à une technologie aussi nouvelle, que Héroult surmonte avec la compétence et la ténacité qui le caractérisent. En 1890, le prix de revient est descendu de 80 F/kg à 15,60 F/kg, un prix suffisamment bas pour entraîner l’arrêt de la production d’aluminium par voie chimique à Salindres. L’avenir est au procédé électrolytique.

Figure 5 : L’atelier d’électrolyse d’aluminium de la SEMF, à Froges, en 1890.
Il s’agit de cuves de deuxième génération, rondes avec sole tournante, afin de briser les croûtes de bain et ainsi faciliter la dissolution de l’alumine.
En 1893, une nouvelle usine de la SEMF est installée et mise en route par Paul Héroult à la Praz, dans la vallée de l’Arc, en amont de Saint-Jean-de-Maurienne (Savoie). Elle est célèbre par la conduite forcée traversant l’Arc en arc de cercle, invention de Paul Héroult imposée par lui malgré les avis unanimement négatifs de ses collaborateurs (fig. 6).

Figure 6 : Usine d’électrolyse d’aluminium de La Praz (Savoie). Franchissement de l’Arc par une conduite forcée autoporteuse, invention de Paul Héroult (1898).
Dès cette même année, la production de la SEMF atteint près de 90 tonnes d’aluminium, avec un prix de revient de 5 F par kg . En 1900, la production mondiale est de près de 5000 tonnes. Mais tout n’est pas joué. Paul Héroult écrit:
L’aluminium n’a pas jusqu’à présent justifié son titre de métal de l’avenir ; il a pris une place modeste dans le commerce des métaux, remplaçant pour des applications particulières tantôt le cuivre, tantôt le fer, l’étain ou le zinc
(23).
Tel est son jugement sur le point où il a conduit le « métal de l’argile ». Il reste à celui-ci à s’imposer, ce à quoi les industriels vont consacrer une inépuisable énergie et des trésors d’imagination : de 1886 à 1993, il a été déposé 264 brevets français s’appuyant sur le procédé de production d’aluminium inventé par Paul Héroult. Ce qui n’empêche pas le texte de son brevet de rester d’une parfaite actualité.
CE N’EST PAS TOUT
Ce serait donner de l’inventeur de génie que fut Paul Héroult une idée limitée que ne pas citer certaines de ses autres découvertes. S’il est hors de propos de parler d’un hélicoptère, d’un hydroglisseur ou d’hypothèses sur la cosmogonie, on ne saurait passer sous silence ce qui fut un deuxième grand succès : le four Héroult, four électrique à deux électrodes en série pour la fabrication de l’acier fondu, instrument classique de l’électrométallurgie, qui vit le jour à La Praz en 1900 et qui fit l’objet de 23 brevets de Paul Héroult. C’est que, comme le dit Paul Séjournet, son ami et collaborateur, dans l’éloge qu’il prononce lors de son décès, en 1914
(…) il avait le rare privilège d’une vue particulièrement précise et nette des nécessités industrielles, un sens pratique admirable, une inlassable persévérance, une aptitude merveilleuse à observer les phénomènes dont il avait provoqué l’apparition et à en tirer les enseignements qu’ils pouvaient comporter
(23).

Figure 7 : Série de cuves d’électrolyse de 175 000 ampères de l’usine Pechiney de Saint-Jean-de-Maurienne, démarrée en 1979.

(1) Pour plus de détails sur cette querelle de brevets, voir C. Pascaud. « Le développement du procédé Hall-Héroult et son accompagnement par la propriété industrielle »,
Cahiers d’histoire de l’aluminium, 20, Paris, 1997, pp. 61-86.
(2) R. Bunsen, « Über die elektrolytische Gewinnung der Erd und Alkali-metalle ».
Poggendorff’s Annalen, 1854, 92, 648-651.
(4) R. Bunsen, « Préparation du magnésium par voie électrolytique ».
Annales de Chimie et de Physique, 36, Paris, 1852, pp. 107-112.
(5) H. Sainte-Claire Deville, « De l’aluminium et de ses composés chimiques ».
Comptes rendus de l’Académie des Sciences, 6 février 1854, pp. 279-280.
(6) H. Sainte-Claire Deville.
De L’aluminium. Ses propriétés, sa fabrication et ses applications, Paris, Mallet-Bachelier, 1859, pp.4-5.
(7) F. Wöhler,
Poggendorff’s Annalen, 11, 1827, pp.144-161.
(8) H. Sainte-Claire Deville, « Nouveau mode de préparation de l’aluminium et de quelques corps simples, métalliques et non métalliques ».
Comptes rendus de l’Académie des Sciences, 10 décembre 1855, pp. 1053-1057.
(9) H. Sainte-Claire Deville,
De L’aluminium. op. cit.
(10) Aujourd’hui Alès (Gard). La ville de Salindres est dans l’arrondissement d’Alès, à quelques kilomètres au nord.
(11) Voir J. Plateau et T. Renaux,
L’aluminium et Paul Morin au Moulin noir. Société d’Histoire de Nanterre, bulletin n° 39, 2007.
(12) P. Héroult. Lettre à sa mère, 1881, Archives des sociétés Rio Tinto – Alcan, Paris.
(13) H. Sainte-Claire Deville.
De l’aluminium. op. cit.p. 95
(14) P. Héroult. « L’aluminium à bon marché »,
Bulletin de la Société de l’industrie minérale, 3e série, t. XIV, Saint-Etienne, 1900. Voir
Cahiers d’histoire de l’aluminium,12, Paris, 1993, pp. 51-58.
(15) Le bronze d’aluminium, alliage de cuivre et d’aluminium (10% d’aluminium le plus souvent) était alors la principale utilisation de l’aluminium. Il avait l’apparence de l’or, et l’on en faisait de l’orfèvrerie de table et de l’orfèvrerie religieuse.
(16) P. Héroult. « L’aluminium à bon marché », op. cit.
(17) Laurent Seigneurin, Communication personnelle.
(18) Voir J. Plateau et Thierry Renaux, op. cit.
(19) « Lettre de Pechiney à Henri Gall, 13 avril 1891 »
in Laurent Seigneurin,
Histoire, op. cit., p. 128.
(20) P. Héroult. « L’aluminium à bon marché », op. cit.
(21) P. Morel. op. cit., pp. 43-44 (contre 1 à 2 tonnes à 80 F/kg vingt ans auparavant)
(22) P. Héroult. « L’aluminium à bon marché », op. cit.
(23) Voir Paul Héroult,
L’Illustration économique et financière, op. cit.
 On produit aujourd’hui annuellement plus de 30 millions de tonnes d’aluminium dans le monde. Toutes sont fabriquées par électrolyse, selon le procédé faisant l’objet d’un brevet accordé à l’ingénieur français Paul Héroult en 1886. C’est dire que ce brevet est le texte fondateur de l’industrie de l’aluminium. Il permet à Héroult et à sa Société électrométallurgique française (SEMF) de lancer les premières fabrications d’aluminium à Froges (Isère) en 1889 puis à La Praz près Saint-Jean de Maurienne (Savoie) en 1893.
On produit aujourd’hui annuellement plus de 30 millions de tonnes d’aluminium dans le monde. Toutes sont fabriquées par électrolyse, selon le procédé faisant l’objet d’un brevet accordé à l’ingénieur français Paul Héroult en 1886. C’est dire que ce brevet est le texte fondateur de l’industrie de l’aluminium. Il permet à Héroult et à sa Société électrométallurgique française (SEMF) de lancer les premières fabrications d’aluminium à Froges (Isère) en 1889 puis à La Praz près Saint-Jean de Maurienne (Savoie) en 1893.